osapiens HUB for Medical Devices
L’échéance d’EUDAMED approche : assurez-vous que vos données UDI soient prêtes avant mai 2026.
Gérez sans effort les données des dispositifs médicaux et produits, garantissez la conformité avec les réglementations internationales et partagez-les de manière transparente avec les hôpitaux, les centrales d'achat et les plateformes de marché. osapiens for Medical Devices assure des processus numériques, automatisés et de haute qualité pour les secteurs de la santé, du médical et du pharmaceutique, dans un environnement validé et sécurisé.

Encore
jours
Votre équipe est-elle prête pour EUDAMED 2026 ? Regardez l’enregistrement de notre dernier webinaire animé par des experts.
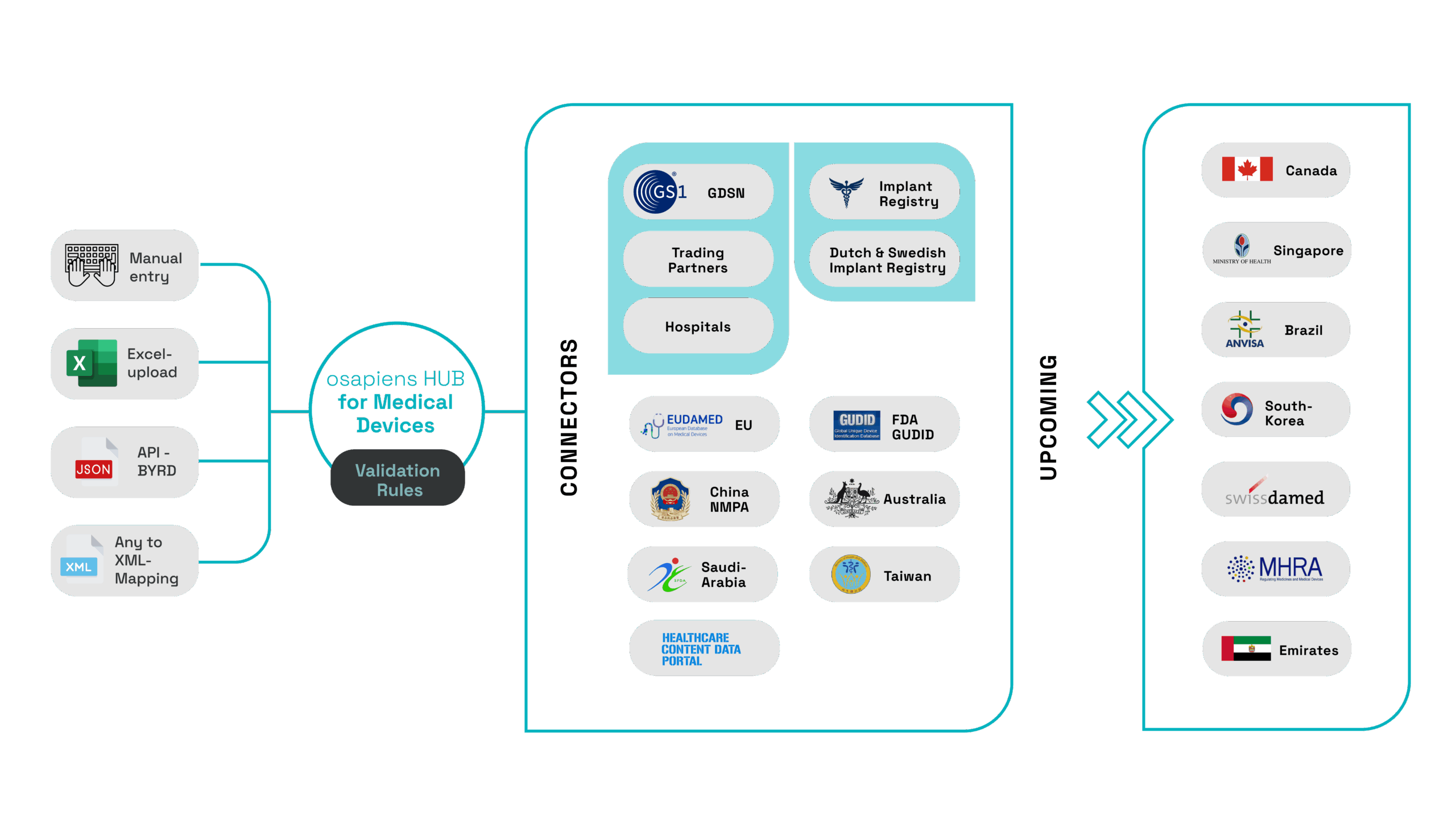
Multiplicité des bases de données réglementaires
Chaque autorité réglementaire dispose de sa propre base de données, et les fabricants de dispositifs médicaux doivent se conformer à différents formats, structures de données, et exigences spécifiques.
Téléchargement complexe des données produits
La transmission des données via les interfaces des autorités réglementaires est souvent complexe, sujette à des erreurs, et manque d’une expérience fluide pour l'utilisateur.
Cohérence des données produits
Fournir des données cohérentes et fiables à toutes les parties prenantes (utilisateurs, hôpitaux, etc.) est crucial pour maintenir la confiance et la transparence autour des dispositifs médicaux.
Centralisez, validez et diffusez vos données sur les dispositifs médicaux
Gérez efficacement les données de vos dispositifs médicaux tout en garantissant la conformité, l’exactitude et la préparation aux audits dans les registres réglementaires mondiaux grâce à l’osapiens HUB for Medical Devices :
✓ Centralisez vos données : Rassemblez toutes les informations produit en un seul endroit afin d’assurer l’alignement entre les équipes internes, les distributeurs et les hôpitaux.
✓ Validez automatiquement : Assurez-vous que vos données UDI et produit répondent aux exigences réglementaires avant soumission, en réduisant au minimum les erreurs et les risques de non-conformité.
✓ Diffusez à l’échelle mondiale : Soumettez efficacement vos données à EUDAMED, au GUDID et à d’autres autorités réglementaires dans le monde entier.
✓ Accélérez la mise sur le marché : Réduisez les frictions dans les échanges de données et commercialisez plus rapidement vos nouveaux produits.
✓ Prêt pour les audits et traçable : Conservez un historique entièrement traçable et exploitable en audit, tout en garantissant la conformité avec le QMS et les normes mondiales.
Notre portefeuille de produits
EUDAMED

Technology Integrations and Partner




Gardez une longueur d’avance sur les exigences réglementaires
Opérez dans un environnement validé et conforme au QMS avec l’osapiens HUB for Medical Devices, afin d’échanger des données UDI de manière sécurisée et conforme entre fabricants, autorités réglementaires et partenaires commerciaux.
Nos experts internes, qui coprésident le groupe d’experts informatiques EUDAMED au sein de MedTech Europe et contribuent à la GS1 Global Healthcare Leadership Team, veillent à ce que votre gestion des données soit alignée sur les réglementations les plus récentes et les meilleures pratiques du secteur.
Guides de conformité
Comment les fabricants de dispositifs médicaux peuvent-ils gérer plus efficacement les données réglementaires sur les produits ? Accédez à des ressources pratiques conçues pour aider les fabricants de dispositifs médicaux à comprendre les exigences réglementaires et à préparer leurs données produit pour les registres mondiaux.
Conformité EUDAMED simplifiée – Votre guide pour une mise en œuvre réussie


Maîtriser la conformité UDI mondiale – Un guide pratique pour les entreprises Medtech.
On-Demand Webinar

EUDAMED 2026 : Ce que les fabricants de dispositifs médicaux doivent faire dès maintenant pour rester sur le marché de l’UE
EUDAMED deviendra obligatoire à compter du 28 mai 2026. C’est l’occasion de comprendre précisément ce que vous devez faire dès maintenant pour rester conforme et éviter des retards coûteux.
Vous souhaitez rester informé ? Regardez gratuitement l’enregistrement de notre dernier webinaire animé par des experts !
osapiens for Medical Devices
Des centaines d'entreprises, dans divers secteurs, font déjà confiance à notre solution.

Centre de ressources