Community
osapeers.org
EUDAMED-Frist rückt näher: Stellen Sie sicher, dass Ihre UDI-Daten vor Mai 2026 bereit sind
Bereiten Sie Ihre Produktdaten für EUDAMED schneller vor – mit einer Plattform, die UDI-Daten automatisch validiert, formatiert und übermittelt. Verwalten und syndizieren Sie Medizinproduktdaten an EUDAMED und weitere globale Register aus einem einzigen System.

Noch
Tage
Jede Aufsichtsbehörde hat ihre eigene Datenbank, und die Hersteller von Medizinprodukten müssen unterschiedliche Datenformate, Datenstrukturen usw. berücksichtigen.
Die Datenbereitstellung über die Schnittstellen der Zulassungsbehörden ist komplex, fehleranfällig und ohne jegliche Kundenerfahrung.
Die Bereitstellung konsistenter Daten für alle Beteiligten (z. B. Anwender, Krankenhäuser usw.) ist der Schlüssel zur Erhaltung des Vertrauens in das Medizinprodukt.
Verwalten Sie Ihre Medizinproduktdaten effizient und stellen Sie dabei Compliance, Genauigkeit und Audit-Bereitschaft über globale regulatorische Register hinweg sicher - mit dem osapiens HUB for Medical Devices:
✓ Zentralisieren Sie Ihre Daten: Erfassen Sie alle Produktinformationen an einem Ort und sorgen Sie dafür, dass interne Teams, Vertriebspartner und Krankenhäuser abgestimmt bleiben.
✓ Automatisch validieren: Stellen Sie sicher, dass Ihre UDI- und Produktdaten vor der Einreichung den regulatorischen Anforderungen entsprechen, und minimieren Sie so Fehler und Compliance-Risiken.
✓ Global übermitteln: Übermitteln Sie Daten effizient an EUDAMED, GUDID und weitere Regulierungsbehörden weltweit.
✓ Time-to-Market beschleunigen: Reduzieren Sie Reibungsverluste im Datenaustausch und bringen Sie neue Produkte schneller auf den Markt.
✓ Audit-sicher und nachvollziehbar: Führen Sie eine vollständig auditierbare Historie und stellen Sie die Einhaltung von QMS-Anforderungen und globalen Standards sicher.
EUDAMED





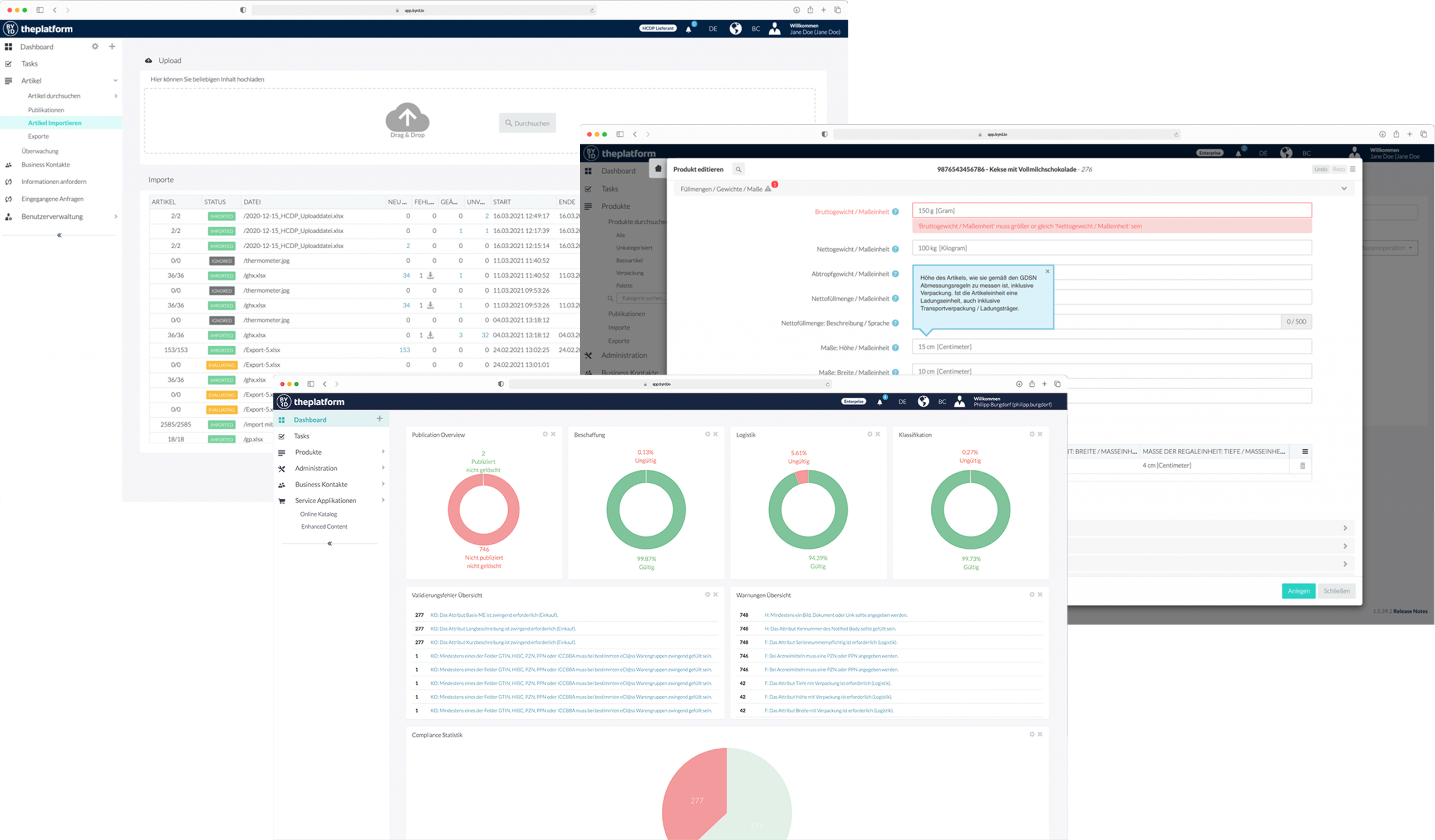
Arbeiten Sie mit dem osapiens HUB for Medical Devices in einer validierten, QMS-konformen Umgebung, um UDI-Daten sicher und regelkonform zwischen Herstellern, Regulierungsbehörden und Handelspartnern auszutauschen.
Unsere internen Experten, die den EUDAMED IT Expert Group bei MedTech Europe mitvorsitzen und zum GS1 Global Healthcare Leadership Team beitragen, stellen sicher, dass Ihr Datenmanagement den neuesten regulatorischen Anforderungen und bewährten Branchenpraktiken entspricht.
Wie können Medizinproduktehersteller regulatorische Produktdaten effektiver verwalten? Greifen Sie auf praxisnahe Ressourcen zu, die Medizinprodukteherstellern dabei helfen, regulatorische Anforderungen zu verstehen und ihre Produktdaten für globale Register vorzubereiten.







Ressourcen Center