Community
osapeers.org
Prepari più rapidamente i suoi dati di prodotto per EUDAMED con una piattaforma che valida, formatta e invia automaticamente i dati UDI. Gestisca e distribuisca i dati dei dispositivi medici a EUDAMED e ad altri registri globali da un unico sistema.

Ancora
giorni
Fornire dati coerenti a tutti gli stakeholder (ad esempio utenti, ospedali, ecc.) è essenziale per mantenere la fiducia nel dispositivo medico.
Gestisca in modo efficiente i dati dei suoi dispositivi medici garantendo al contempo conformità, accuratezza e preparazione agli audit nei registri regolatori globali con osapiens HUB for Medical Devices:
✓ Centralizzi i suoi dati: raccolga tutte le informazioni di prodotto in un unico luogo, mantenendo allineati team interni, distributori e ospedali.
✓ Validi automaticamente: si assicuri che i suoi dati UDI e di prodotto soddisfino i requisiti normativi prima dell’invio, riducendo al minimo errori e rischi di conformità.
✓ Distribuisca a livello globale: invii i dati in modo efficiente a EUDAMED, GUDID e ad altre autorità regolatorie in tutto il mondo.
✓ Acceleri il time-to-market: riduca gli attriti nello scambio di dati e porti più rapidamente sul mercato nuovi prodotti.
✓ Pronto per gli audit e tracciabile: mantenga uno storico completamente verificabile e garantisca la conformità al QMS e agli standard globali.
EUDAMED





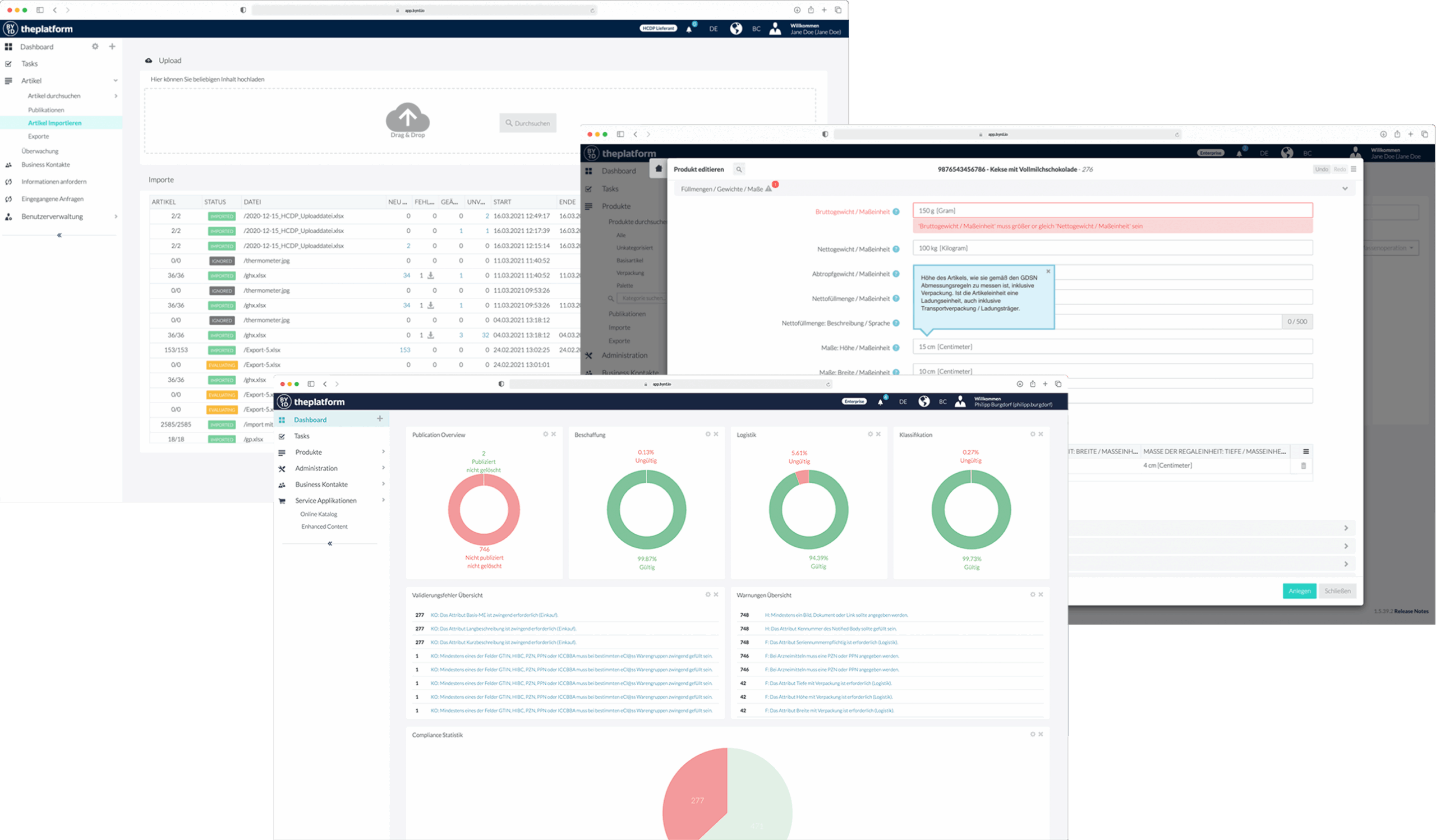
Operi in un ambiente validato e conforme al QMS con osapiens HUB for Medical Devices, per scambiare dati UDI in modo sicuro e conforme tra produttori, autorità regolatorie e partner commerciali.
I nostri esperti interni, che co-presiedono l’EUDAMED IT Expert Group di MedTech Europe e contribuiscono al GS1 Global Healthcare Leadership Team, garantiscono che la sua gestione dei dati sia allineata alle normative più recenti e alle migliori pratiche del settore.
Come possono i produttori di dispositivi medici gestire in modo più efficace i dati regolatori sui prodotti? Acceda a risorse pratiche pensate per aiutare i produttori di dispositivi medici a comprendere i requisiti normativi e a preparare i propri dati di prodotto per i registri globali.



EUDAMED 2026: Cosa devono fare ora i produttori di dispositivi medici per rimanere sul mercato dell’UE
EUDAMED diventerà obbligatorio il 28 maggio 2026. Questa è la vostra occasione per capire esattamente cosa dovete fare ora per rimanere conformi ed evitare costosi ritardi.
Vuoi rimanere aggiornato? Guarda gratuitamente la registrazione del nostro ultimo webinar tenuto da esperti!




Centro risorse