Community
osapeers.org
Gestite con facilità i dati relativi a dispositivi e prodotti medici, garantite la conformità alle normative globali e condivideteli senza difficoltà con ospedali, gruppi di acquisto e marketplace. La soluzione osapiens per Dispositivi Medici assicura processi digitali, automatizzati e certificati per il settore sanitario, medico e farmaceutico, all’interno di un ambiente convalidato.

Ancora
giorni
EUDAMED
In entrambi i casi, il vostro progetto sarà seguito dal team più esperto del settore. Vi aiutiamo a comprendere, attributo per attributo, cosa è richiesto e come rispettare i requisiti normativi.
Se avete già portato a termine un progetto GUDID per la FDA statunitense, vi supportiamo nell’identificare le differenze strutturali e normative tra i due sistemi, compresa l’organizzazione dei dati EUDAMED tramite BUDI.
Contattateci oggi stesso per una demo o per confrontarci sul piano progettuale più adatto alla vostra organizzazione.



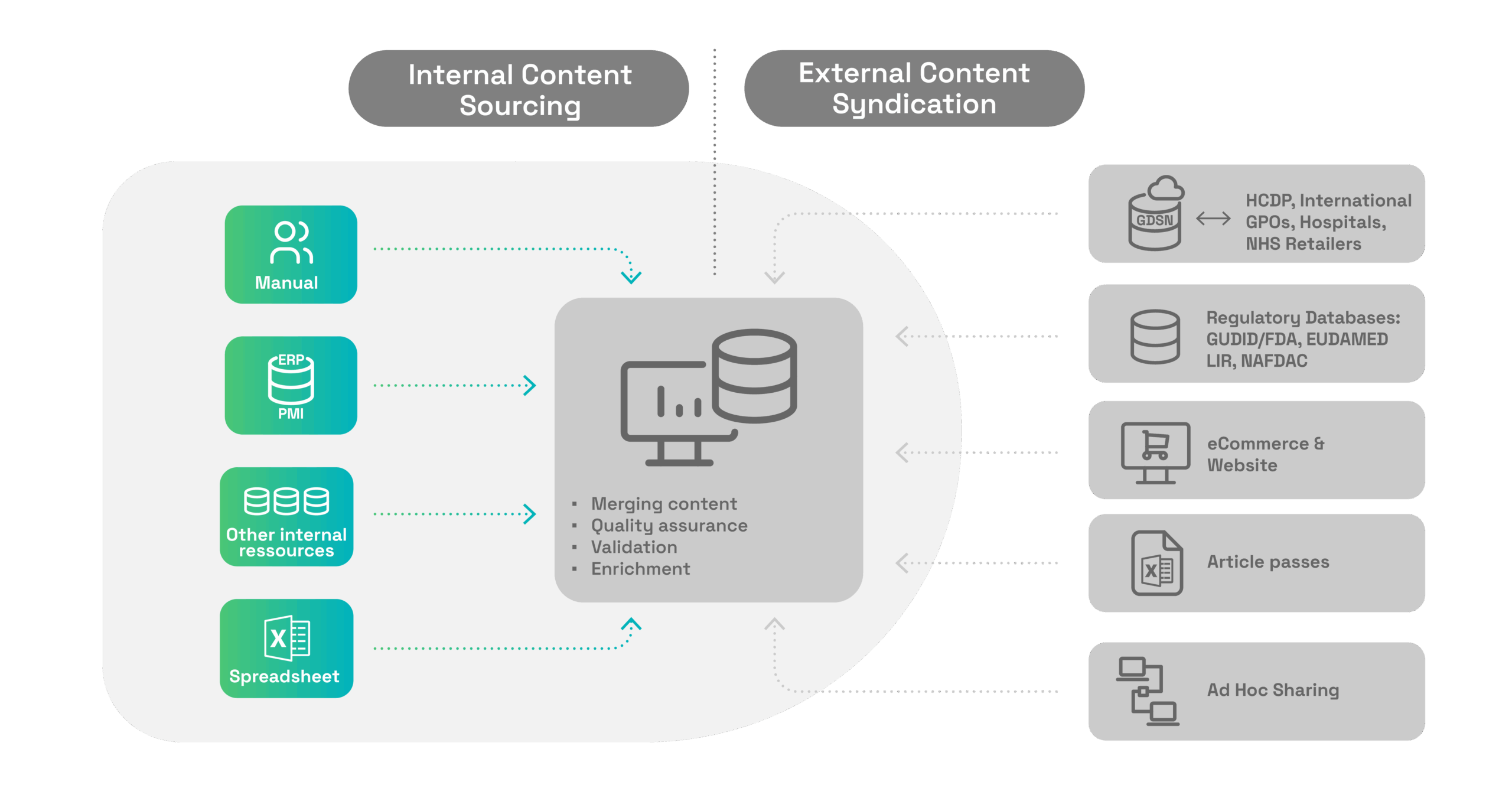
Nel settore sanitario, la gestione delle informazioni di prodotto richiede l’adozione di formati dati e protocolli complessi per l’uso interno, lo scambio di dati e il rispetto di rigorosi standard di qualità all’interno di un ambiente convalidato. Promuovendo un’assistenza sanitaria affidabile attraverso uno scambio di dati fluido e strutturato, osapiens for Medical Devices rende possibile la condivisione dei dati dei dispositivi medici dai produttori verso i database normativi e i partner commerciali a livello globale. Regolamenti e standard come COVIN, GDSN, EUDAMED, GUDID, LIR, US FDA e altri sono pensati per migliorare la qualità dei dati, garantirne la tracciabilità e supportare processi digitali per una gestione conforme e basata su standard di qualità.
osapiens for Medical Devices ottimizza il trasferimento dei dati relativi ai dispositivi medici, garantendo uno scambio fluido tra produttori, database normativi e partner commerciali in tutto il mondo. La soluzione di integrazione dati osapiens vi consente di gestire le informazioni di prodotto senza sforzo, mentre il connettore osapiens garantisce la conformità automatica dei vostri dati ai formati richiesti dalle autorità di vigilanza di tutto il mondo. Eliminate gli ostacoli nello scambio di dati e conquistate la fiducia dei vostri partner e clienti.
Fornire dati coerenti a tutti gli stakeholder (ad esempio utenti, ospedali, ecc.) è essenziale per mantenere la fiducia nel dispositivo medico.
La piattaforma osapiens supporta molteplici modalità di trasferimento dati, tra cui connessioni da Macchina a Macchina (XML via AS/2, API, JSON), caricamento di file Excel e inserimento manuale. osapiens consente di gestire dati e distribuzione da un’unica piattaforma, collegandovi a GS1/GDSN, EUDAMED, FDA GUDID, GUID, TGA Australia, Swissmedic, Emirates Health Services (EHS), Dubai Health Authority (DHA) e molte altre.
Ci impegniamo a garantire la connettività tra osapiens e tutte le entità federali con database UDI. In futuro, quando i seguenti sistemi normativi saranno pienamente operativi, prevediamo di estendere la connettività anche a: Colombia/INVIMA, Brasile/ANVISA, Regno Unito/NHS e MHRA, Canada e Singapore.
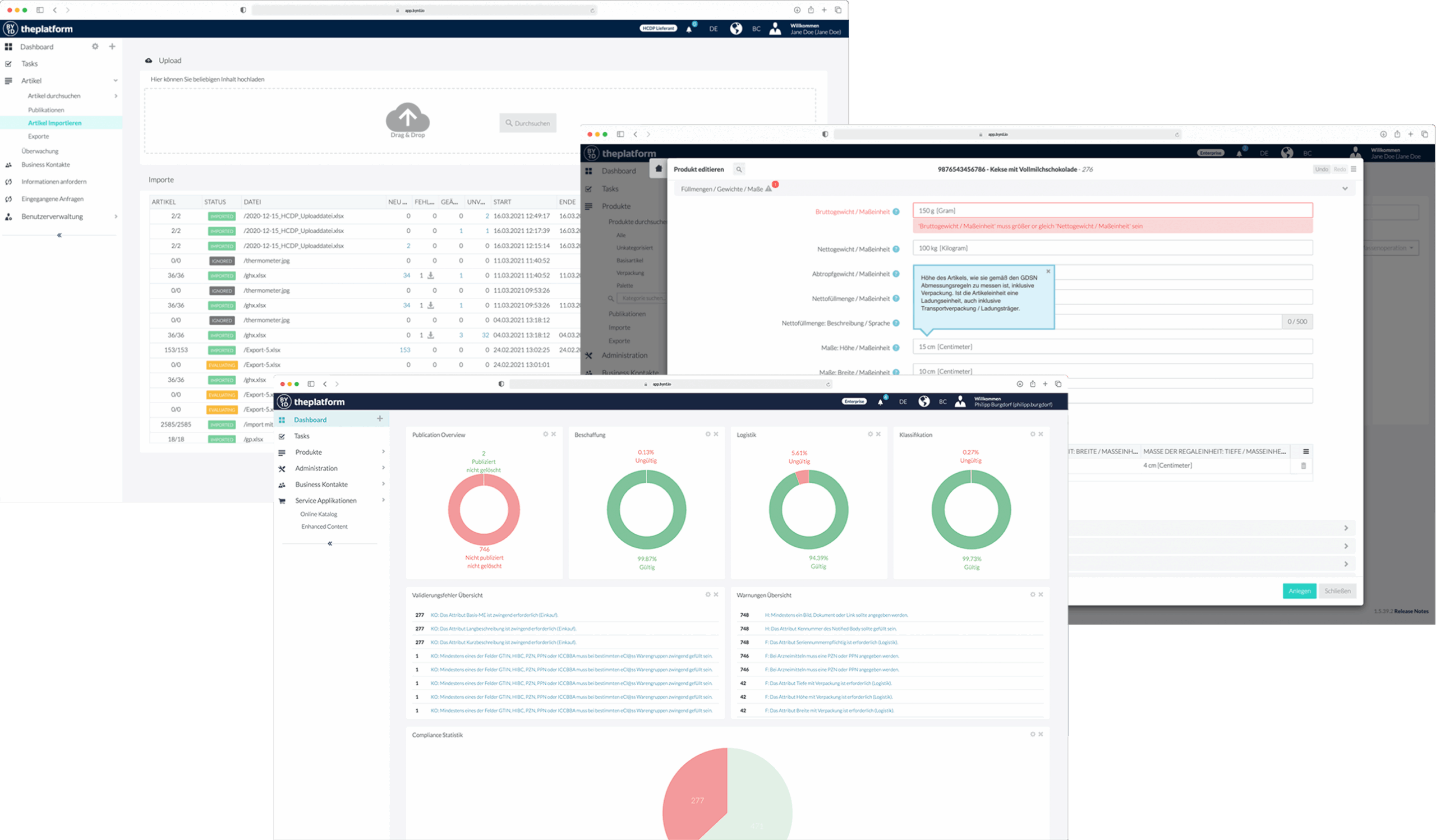
osapiens for Medical Devices supporta l'intero Product Content Life Cycle Management
Aggregazione
L’aggregazione dei contenuti e dei dati di prodotto all’interno della soluzione osapiens for Medical Devices consente di gestire in modo centralizzato tutte le informazioni richieste e mantenerle conformi a livello globale. Aggregando i vostri dati, garantite che i vostri dispositivi rispettino tutti i requisiti normativi, in modo efficiente e senza errori.
Vantaggi dell’aggregazione dei dati di prodotto:
Sfruttate i vantaggi dell’aggregazione centralizzata dei dati e assicurate una gestione efficiente e conforme dei vostri dispositivi medici. Rimanete conformi all’UDI e massimizzate la vostra efficienza!